[앵커]
BMS가 최근 항암제 전문 기업 ‘터닝포인트 테라퓨틱스’를 무려 5조원에 인수해 눈길을 끌었는데요. 터닝포인트가 보유한 비소세포성 폐암 치료제 ‘레포트렉티닙’의 가치를 그만큼 높게 평가한 겁니다. 그런데, 국내에도 같은 후보물질을 개발 중인 기업이 있죠. 바로 ‘뉴지랩파마’입니다. 한신영 상무는 자사의 탈레트렉티닙이 레포트렉티닙보다 객관적 반응률이 더 우수하다고 자신합니다. 김효선 기자가 한 상무를 만나 개발 진행 상황을 들어봤습니다.
[기자]
뉴지랩파마의 탈레트렉티닙은 현재 한·미·일 글로벌 임상을 진행 중인데요. 특히 국내에서는 모든 폐암 환자들로까지 임상범위가 확대 돼 임상기간 단축, 시장성 확장 등이 예상돼 큰 기대를 모으고 있습니다. 자세한 진행 상황, 들어봤습니다.

Q. 터닝포인트의 ‘레포트렉티닙’ 과 뉴지랩파마의 ‘탈레트렉티닙’ 차별점은?
[한신영/ 뉴지랩파마 사업개발 상무]
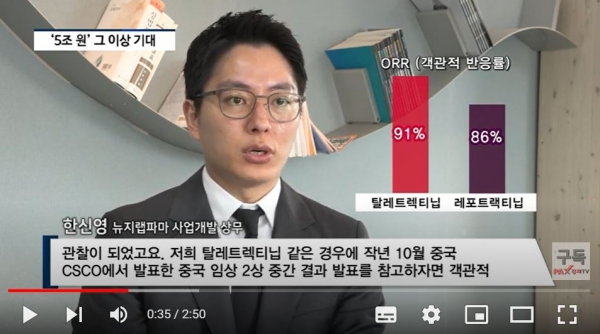
“터닝포인트가 현재 개발하고 있는 레포트랙티닙의 경우 치료 경험이 없는 환자군에서 1차 치료군이라고 하는데 객관적 반응률인 ORR이 86%으로 관찰이 되었고요. 저희 탈레트렉티닙 같은 경우에 작년 10월 중국 CSCO에서 발표한 중국 임상 2상 중간 결과 발표를 참고하자면 객관적 반응률이 91%로 관찰이 됐습니다. 그래서 퍼센테이지 상의 수치로 봤을때는 91% VS 86%로 저희 약물이 근소하게 앞선다고 볼 수 있는데요. 이외에도 중요한 지표로 여겨지는 중앙 무진행생존기간인 mPFS라는 지표가 있습니다. 그 지표에서는 저희 약물이 29.1개월, 그리고 레포트랙티닙이 24.6개월로 관찰이 되어서 총 4.5개월의 무진행생존 기간이 차이가 있는 것으로 나타났습니다. 약 1-2개월의 차이도 큰 의미로 받아들여지고 있는 만큼 탈레트렉티닙이 레포트랙티닙 대비 월등히 우월한 유효성을 가지고 있다고 판단하고 있습니다.”
Q.현재 진행상황 및 상용화 시점, 기대하는 바는?
[한신영/ 뉴지랩파마 사업개발 상무]
“일단 탈레트렉티닙이 대상으로 하고 있는 환자군이 비소세포성폐암 ROS1 유전자 변이군은 국내에서 희귀의약품 지정 요건에 해당 합니다. 그렇기 때문에 저희가 지금 현재 진행하고 있는 임상이 22년 연내에 120명 규모로 모집을 완료할 경우에는 국내에서 조건부사용 승인을 전제로 24년도 1분기에는 국내 신약허가 승인을 취득할 수 있을것으로 현재 예상하고 있고요. 시장 규모적인 측면을 봤을 때 2019년도에 발표된 (전세계) 폐암치료제 시장 규모는 25조원 정도로 추산되고 있습니다. 그중에 크리조티닙의 국내 매출액이 약 500억 원 정도로 지금 추산이 되고 있는데요. 탈레트렉티닙의 경우에는 크리조티닙과 직접 경쟁하는 1차 치료제 뿐 만 아니라 크리조티닙 복약 후에 내성 환자들을 대상으로 하는 2차 치료제군까지 모두 대상으로 하고 있기 때문에 크리조티닙의 국내 매출액인 500억 원 정도는 국내에서 무난히 달성 할 수 있을 것으로 예상하고 있습니다.”

Q. 국내 임상 진행상황 및 경쟁력은?
[한신영/ 뉴지랩파마 사업개발 상무]
“이미 발표된 탈레트렉티닙의 데이터를 보면 국내 신약 허가 승인에는 무리가 없을 정도로 긍정적으로 판단을 하고 있고요. 이미 1차 치료제로 승인을 받아서 판매를 하고 있는 크리조티닙과 엔트렉티닙의 경우 승인 당시에 객관적 반응률이 78%정도로 관찰이 되었고, 이는 저희가 앞서 말씀 드렸던 91%와의 수치와는 일정 부분 이상의 차이가 있기 때문에 탈레트렉티닙의 유효성이 더 우월할 수 있다고 저희는 판단하고 있습니다.

그리고 그 이외에도 탈레트렉티닙은 1상 시험과 2상 시험을 거쳐서 뇌전이 병변에 대한 치료 효과가 여러건 입증이 된 부분이 있어요. 그래서 그 부분에 크리조티닙이 없는 부분이기 때문에 크리조티닙 대비해서 탈레트렉티닙이 시장 진입을 한다면 훨씬 더 우월 할 것으로 예상을 하고 있습니다. 그렇기 때문에 저희 약물의 신약허가 승인을 취득한다면 비소세포성폐암 ROS1 유전자 변이 환자들에게 새로운 치료 옵션과 희망을 드릴 수 있을 것으로 예상합니다.”

